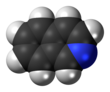
Isochinolin - Isoquinoline

|
|||
|
|
|||
| Namen | |||
|---|---|---|---|
|
Bevorzugter IUPAC-Name
Isochinolin |
|||
| Andere Namen
Benzo[ c ]pyridin
2-Benzazin |
|||
| Identifikatoren | |||
|
3D-Modell ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Arzneimittelbank | |||
| ECHA-InfoCard |
100.003.947 |
||
| EG-Nummer | |||
|
PubChem- CID
|
|||
| UNII | |||
|
CompTox-Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eigenschaften | |||
| C 9 H 7 N | |||
| Molmasse | 129,162 g·mol -1 | ||
| Aussehen | Farblose ölige Flüssigkeit; hygroskopische Blutplättchen, wenn sie fest sind | ||
| Dichte | 1,099 g / cm 3 | ||
| Schmelzpunkt | 26–28 °C (79–82 °F; 299–301 K) | ||
| Siedepunkt | 242 °C (468 °F; 515 K) | ||
| Säure (p K a ) | pK BH + = 5,14 | ||
| –83,9·10 –6 cm 3 /mol | |||
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Infobox-Referenzen | |||
Isochinolin ist eine heterozyklische aromatische organische Verbindung . Es ist ein Strukturisomer von Chinolin . Isochinolin und Chinolin sind Benzopyridine , die aus einem an einen Pyridinring kondensierten Benzolring bestehen . Im weiteren Sinne wird der Begriff Isochinolin verwendet, um auf Isochinolin- Derivate Bezug zu nehmen . 1-Benzylisochinolin ist das strukturelle Rückgrat in natürlich vorkommenden Alkaloiden, einschließlich Papaverin . Der Isochinolinring dieser Naturstoffe leitet sich von der aromatischen Aminosäure Tyrosin ab .
Eigenschaften
Isochinolin ist bei Temperaturen oberhalb seines Schmelzpunktes eine farblose hygroskopische Flüssigkeit mit penetrantem, unangenehmem Geruch . Unreine Proben können bräunlich erscheinen, wie es für Stickstoffheterocyclen typisch ist. Es kristallisiert in Plättchen, die eine geringe Löslichkeit in Wasser haben, sich aber gut in Ethanol , Aceton , Diethylether , Schwefelkohlenstoff und anderen üblichen organischen Lösungsmitteln lösen . Als protoniertes Derivat ist es auch in verdünnten Säuren löslich .
Ein Seine analog Pyridin, Isochinolin ist eine schwache Base , mit einem p K a von 5,14. Es protoniert bei Behandlung mit starken Säuren wie HCl , um Salze zu bilden . Es bildet Addukte mit Lewis-Säuren wie BF 3 .
Produktion
Isochinolin wurde erstmals 1885 von Hoogewerf und van Dorp aus Steinkohlenteer isoliert . Sie isolierten es durch fraktionierte Kristallisation des Säuresulfats. Weissgerber entwickelte 1914 einen schnelleren Weg durch die selektive Gewinnung von Steinkohlenteer, wobei er sich die Tatsache zunutze machte, dass Isochinolin basischer ist als Chinolin. Aus dem Gemisch kann dann Isochinolin durch fraktionierte Kristallisation des Säuresulfats isoliert werden.
Obwohl Isochinolin-Derivate durch mehrere Verfahren synthetisiert werden können, liefern relativ wenige direkte Verfahren das unsubstituierte Isochinolin. Die Pomeranz-Fritsch-Reaktion bietet eine effiziente Methode zur Herstellung von Isochinolin. Bei dieser Reaktion wird ein Benzaldehyd und ein Aminoacetoaldehyddiethylacetal verwendet, die in einem sauren Medium zu Isochinolin reagieren. Alternativ Benzylamin und Glyoxal Acetal kann verwendet werden, um das gleiche Ergebnis mit der Schlittler Müller-Modifikation herzustellen.
Mehrere andere Verfahren sind für die Herstellung verschiedener Isochinolin-Derivate nützlich.
Bei der Bischler-Napieralski-Reaktion wird ein β- Phenylethylamin mit einer Lewis-Säure wie Phosphorylchlorid oder Phosphorpentoxid acyliert und cyclodehydratisiert . Das resultierende 1-substituierte 3,4-Dihydroisochinolin kann dann mit Palladium dehydriert werden. Die folgende Bischler-Napieralski-Reaktion produziert Papaverin.
Die Pictet-Gams-Reaktion und die Pictet-Spengler-Reaktion sind beides Variationen der Bischler-Napieralski-Reaktion. Eine Pictet-Gams-Reaktion funktioniert ähnlich wie die Bischler-Napieralski-Reaktion; der einzige Unterschied besteht darin, dass eine zusätzliche Hydroxygruppe im Reaktanten eine Stelle für die Dehydratisierung unter den gleichen Reaktionsbedingungen wie die Cyclisierung bereitstellt, um das Isochinolin zu ergeben, anstatt eine separate Reaktion zu erfordern, um ein Dihydroisochinolin-Zwischenprodukt umzuwandeln.
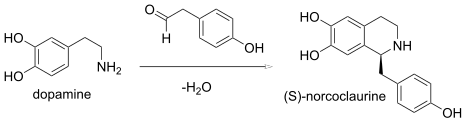
In einer Pictet-Spengler-Reaktion entsteht durch Kondensation eines β- Phenylethylamins und eines Aldehyds ein Imin, das anstelle des Dihydroisochinolins zu einem Tetrahydroisochinolin cyclisiert wird . In der Enzymologie ist die (S) -Norcoclaurinsynthase ( EC 4.2.1.78 ) ein Enzym , das eine biologische Pictect-Spengler-Synthese katalysiert :
Auch intramolekulare Aza-Wittig-Reaktionen liefern Isochinolinen.
Anwendungen von Derivaten
Isochinolinen finden viele Anwendungen, darunter:
- Anästhetika; Dimethisoquin ist ein Beispiel (siehe unten).
- Antihypertoniemittel wie Quinapril und Debrisoquin (alle abgeleitet von 1,2,3,4-Tetrahydroisochinolin).
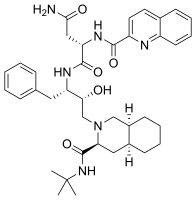
- antiretrovirale Mittel, wie Saquinavir mit einer funktionellen Isochinolylgruppe (siehe unten).
- Vasodilatatoren, ein bekanntes Beispiel, Papaverin , unten gezeigt.
Bisbenzylisochinoliniumverbindungen sind Verbindungen mit ähnlicher Struktur wie Tubocurarin . Sie haben zwei Isochinoliniumstrukturen, die durch eine Kohlenstoffkette verbunden sind und zwei Esterbindungen enthalten .
Im menschlichen Körper
Die Parkinson-Krankheit , eine langsam fortschreitende Bewegungsstörung, wird vermutlich durch bestimmte Neurotoxine verursacht . Ein Neurotoxin namens MPTP (1[ N ]-Methyl-4-phenyl-1,2,3,6- tetrahydropyridin ), die Vorstufe von MPP + , wurde in den 1980er Jahren gefunden und mit der Parkinson-Krankheit in Verbindung gebracht. Die aktiven Neurotoxine zerstören dopaminerge Neuronen , was zu Parkinsonismus und Parkinson-Krankheit führt. Es wurde festgestellt, dass mehrere Tetrahydroisochinolin- Derivate die gleichen neurochemischen Eigenschaften wie MPTP aufweisen. Diese Derivate können als Vorläufer für aktive Neurotoxine wirken.
Andere Verwendungen
Isochinolinen werden bei der Herstellung von Farbstoffen , Farben , Insektiziden und Antimykotika verwendet . Es wird auch als Lösungsmittel zur Extraktion von Harzen und Terpenen sowie als Korrosionsinhibitor verwendet .
Siehe auch
- Naphthalin , ein Analogon ohne das Stickstoffatom.
Verweise
Externe Links
. Encyclopædia Britannica . 22 (11. Aufl.). 1911. S. 758–759.