Fettsäuresynthese - Fatty acid synthesis
Die Fettsäuresynthese ist die Bildung von Fettsäuren aus Acetyl-CoA und NADPH durch die Wirkung von Enzymen, die als Fettsäuresynthasen bezeichnet werden . Dieser Vorgang findet im Zytoplasma der Zelle statt . Der größte Teil des in Fettsäuren umgewandelten Acetyl-CoA wird über den glykolytischen Weg aus Kohlenhydraten gewonnen . Der glykolytische Weg liefert auch das Glycerin, mit dem sich drei Fettsäuren (mittels Esterbindungen ) zu Triglyceriden (auch bekannt als „Triacylglycerine“ – zur Unterscheidung von „Fettsäuren“ – oder einfach als „Fett“ verbinden können), die Endprodukt des lipogenen Prozesses. Wenn sich nur zwei Fettsäuren mit Glycerin verbinden und die dritte Alkoholgruppe mit einer Gruppe wie Phosphatidylcholin phosphoryliert wird , wird ein Phospholipid gebildet. Phospholipide bilden den Großteil der Lipiddoppelschichten , die die Zellmembranen bilden und die Organellen innerhalb der Zellen umgeben (z. B. Zellkern , Mitochondrien , endoplasmatisches Retikulum , Golgi-Apparat usw.)
Geradkettige Fettsäuren
Geradkettige Fettsäuren kommen in zwei Arten vor: gesättigt und ungesättigt.
Gesättigte geradkettige Fettsäuren
Ähnlich wie bei der β-Oxidation erfolgt die Synthese von geradkettigen Fettsäuren über die unten gezeigten sechs wiederkehrenden Reaktionen, bis die 16-Kohlenstoff- Pamitinsäure produziert wird.
Die dargestellten Diagramme zeigen, wie Fettsäuren in Mikroorganismen synthetisiert werden und listen die Enzyme auf, die in Escherichia coli vorkommen . Diese Reaktionen werden von der Fettsäure-Synthase II (FASII) durchgeführt, die im Allgemeinen mehrere Enzyme enthält, die als ein Komplex wirken. FASII kommt in Prokaryoten , Pflanzen, Pilzen und Parasiten sowie in Mitochondrien vor .
Bei Tieren sowie bei einigen Pilzen wie Hefe treten dieselben Reaktionen an der Fettsäuresynthase I (FASI) auf, einem großen dimeren Protein, das alle enzymatischen Aktivitäten aufweist, die zur Bildung einer Fettsäure erforderlich sind. FASI ist weniger effizient als FASII; es ermöglicht jedoch die Bildung von mehr Molekülen, einschließlich "mittelkettiger" Fettsäuren über einen frühen Kettenabbruch.
Sobald eine 16:0-Kohlenstoff-Fettsäure gebildet wurde, kann sie eine Reihe von Modifikationen erfahren, die zu einer Entsättigung und/oder Verlängerung führen. Die Elongation, beginnend mit Stearat (18:0), erfolgt hauptsächlich im ER durch mehrere membrangebundene Enzyme. Die am Elongationsverfahren beteiligten enzymatischen Schritte sind im Prinzip die gleichen wie bei FAS, aber die vier wichtigsten aufeinander folgenden Schritte der Elongation werden von einzelnen Proteinen durchgeführt, die physikalisch verbunden sein können.
| Schritt | Enzym | Reaktion | Beschreibung |
|---|---|---|---|
| (ein) | Acetyl-CoA:ACP-Transacylase | Aktiviert Acetyl-CoA für die Reaktion mit Malonyl-ACP | |
| (b) | Malonyl-CoA:ACP-Transacylase |
|
Aktiviert Malonyl-CoA für die Reaktion mit Acetyl-ACP |
| (c) | 3-Ketoacyl-ACP-Synthase | Reagiert ACP-gebundene Acylkette mit kettenverlängernder Malonyl-ACP | |
| (d) | 3-Ketoacyl-ACP-Reduktase | Reduziert das Kohlenstoff-3-Keton zu einer Hydroxylgruppe | |
| (e) | 3-Hydroxyacyl-ACP-Dehydrase | Eliminiert Wasser | |
| (f) | Enoyl-ACP-Reduktase | Reduziert die C2-C3-Doppelbindung. | |
| Abkürzungen: ACP – Acyl Carrier Protein , CoA – Coenzym A , NADP – Nicotinamid-Adenin-Dinukleotid-Phosphat . | |||
Beachten Sie, dass während der Fettsynthese das Reduktionsmittel NADPH ist , während NAD das Oxidationsmittel bei der Beta-Oxidation (dem Abbau von Fettsäuren zu Acetyl-CoA) ist. Dieser Unterschied veranschaulicht ein allgemeines Prinzip, dass NADPH bei biosynthetischen Reaktionen verbraucht wird, während NADH bei energieliefernden Reaktionen erzeugt wird. (Daher wird NADPH auch für die Synthese von Cholesterin aus Acetyl-CoA benötigt, während NADH während der Glykolyse gebildet wird .) Die Quelle des NADPH ist zweifach. Wenn Malat durch "NADP + -gebundenes Malic-Enzym" oxidativ decarboxyliert wird , um Pyruvat zu bilden , werden CO 2 und NADPH gebildet. NADPH wird auch durch den Pentosephosphatweg gebildet , der Glucose in Ribose umwandelt, die bei der Synthese von Nukleotiden und Nukleinsäuren verwendet werden kann , oder es kann zu Pyruvat katabolisiert werden.
Umwandlung von Kohlenhydraten in Fettsäuren
Beim Menschen werden Fettsäuren vor allem in der Leber und im Fettgewebe sowie in den Milchdrüsen während der Stillzeit aus Kohlenhydraten gebildet .
Das bei der Glykolyse produzierte Pyruvat ist ein wichtiger Vermittler bei der Umwandlung von Kohlenhydraten in Fettsäuren und Cholesterin. Dies geschieht über die Umwandlung von Pyruvat in Acetyl-CoA im Mitochondrium. Dieses Acetyl-CoA muss jedoch in das Zytosol transportiert werden, wo die Synthese von Fettsäuren und Cholesterin stattfindet. Dies kann nicht direkt erfolgen. Um zytosolisches Acetyl-CoA zu erhalten, wird Citrat (hergestellt durch die Kondensation von Acetyl-CoA mit Oxalacetat) aus dem Zitronensäurezyklus entfernt und über die innere mitochondriale Membran in das Zytosol transportiert. Dort wird es durch ATP-Citrat-Lyase in Acetyl-CoA und Oxalacetat gespalten. Das Oxalacetat kann zur Gluconeogenese (in der Leber) verwendet werden oder als Malat in die Mitochondrien zurückgeführt werden. Das zytosolische Acetyl-CoA wird durch Acetyl-CoA-Carboxylase zu Malonyl- CoA carboxyliert , dem ersten Schritt in der Synthese von Fettsäuren.
Tiere können keine Kohlenhydrate aus Fettsäuren wieder synthetisieren
Der Hauptbrennstoff, der im Körper von Tieren gespeichert wird, ist Fett. Die Fettreserven eines jungen erwachsenen Menschen liegen durchschnittlich zwischen 15 und 20 kg, variieren jedoch stark je nach Alter, Geschlecht und individueller Veranlagung. Im Gegensatz dazu speichert der menschliche Körper nur etwa 400 g Glykogen , von denen 300 g in der Skelettmuskulatur eingeschlossen sind und dem Körper als Ganzes nicht zur Verfügung stehen. Die etwa 100 g Glykogen, die in der Leber gespeichert sind, sind innerhalb eines Tages nach dem Hungern aufgebraucht. Danach muss die Glukose, die von der Leber zur allgemeinen Verwendung durch das Körpergewebe ins Blut freigesetzt wird, aus den glucogenen Aminosäuren und einigen anderen gluconeogenen Substraten synthetisiert werden , die keine Fettsäuren enthalten.
Fettsäuren werden innerhalb der Mitochondrien durch Beta-Oxidation zu Acetyl-CoA abgebaut , während Fettsäuren außerhalb des Mitochondriums, im Zytosol, aus Acetyl-CoA synthetisiert werden. Die beiden Reaktionswege unterscheiden sich nicht nur darin, wo sie stattfinden, sondern auch in den Reaktionen, die ablaufen, und den verwendeten Substraten. Die beiden Pfade hemmen sich gegenseitig und verhindern, dass das durch Beta-Oxidation produzierte Acetyl-CoA über die Acetyl-CoA-Carboxylase- Reaktion in den Synthesepfad eindringt . Es kann auch nicht in Pyruvat umgewandelt werden, da die Pyruvat-Decarboxylierungsreaktion irreversibel ist. Stattdessen kondensiert es mit Oxalacetat , um in den Zitronensäurezyklus einzutreten . Während jeder Umdrehung des Zyklus verlassen zwei Kohlenstoffatome den Zyklus als CO 2 in den Decarboxylierungsreaktionen, die durch Isocitrat-Dehydrogenase und alpha-Ketoglutarat-Dehydrogenase katalysiert werden . Somit oxidiert jede Umdrehung des Zitronensäurezyklus eine Acetyl-CoA-Einheit, während das Oxalacetat-Molekül regeneriert wird, mit dem sich das Acetyl-CoA ursprünglich zu Zitronensäure verbunden hatte . Die Decarboxylierungsreaktionen finden statt, bevor Malat im Zyklus gebildet wird. Malat ist die einzige Substanz, die aus dem Mitochondrium entfernt werden kann, um in den glukoneogenen Weg einzutreten , um in der Leber oder jedem anderen Gewebe Glukose oder Glykogen zu bilden. Es kann daher keine Nettoumwandlung von Fettsäuren in Glucose erfolgen.
Nur Pflanzen besitzen die Enzyme, um Acetyl-CoA in Oxalacetat umzuwandeln, aus dem Malat gebildet und schließlich in Glukose umgewandelt werden kann.
Verordnung
Acetyl-CoA wird durch Acetyl-CoA-Carboxylase zu Malonyl-CoA gebildet , an welchem Punkt Malonyl-CoA dazu bestimmt ist, in den Fettsäuresyntheseweg einzuspeisen. Die Acetyl-CoA-Carboxylase ist der Regulationspunkt bei der Synthese gesättigter geradkettiger Fettsäuren und unterliegt sowohl der Phosphorylierung als auch der allosterischen Regulation . Die Regulation durch Phosphorylierung findet hauptsächlich bei Säugetieren statt, während die allosterische Regulation bei den meisten Organismen vorkommt. Die allosterische Kontrolle erfolgt als Rückkopplungshemmung durch Palmitoyl-CoA und Aktivierung durch Citrat. Bei hohen Konzentrationen von Palmitoyl-CoA, dem Endprodukt der Synthese gesättigter Fettsäuren, inaktiviert es allosterisch die Acetyl-CoA-Carboxylase, um eine Ansammlung von Fettsäuren in den Zellen zu verhindern. Citrat aktiviert die Acetyl-CoA-Carboxylase bei hohen Spiegeln, da hohe Spiegel darauf hinweisen, dass genügend Acetyl-CoA vorhanden ist, um in den Krebs-Zyklus einzuspeisen und Energie zu sparen.
Hohe Plasmaspiegel von Insulin im Blutplasma (z. B. nach den Mahlzeiten) bewirken die Dephosphorylierung der Acetyl-CoA-Carboxylase und fördern so die Bildung von Malonyl-CoA aus Acetyl-CoA und damit die Umwandlung von Kohlenhydraten in Fettsäuren, während Adrenalin und Glucagon (wird bei Hunger und körperlicher Betätigung ins Blut freigesetzt) bewirken die Phosphorylierung dieses Enzyms, wodurch die Lipogenese zugunsten der Fettsäureoxidation durch Beta-Oxidation gehemmt wird .
Ungesättigte geradkettige Fettsäuren
Anaerobe Entsättigung
Viele Bakterien nutzen den anaeroben Weg zur Synthese ungesättigter Fettsäuren. Dieser Weg verwendet keinen Sauerstoff und ist abhängig von Enzymen, um die Doppelbindung vor der Verlängerung unter Verwendung der normalen Fettsäuresynthesemaschinerie einzufügen. Bei Escherichia coli ist dieser Weg gut verstanden.
- FabA ist eine β-Hydroxydecanoyl-ACP-Dehydrase – sie ist spezifisch für das Zwischenprodukt der Synthese von gesättigten Fettsäuren mit 10 Kohlenstoffatomen (β-Hydroxydecanoyl-ACP).
- FabA katalysiert die Dehydratisierung von β-Hydroxydecanoyl-ACP, was die Freisetzung von Wasser und die Insertion der Doppelbindung zwischen C7 und C8 vom Methylende aus bewirkt. Dadurch entsteht das trans-2-Decenoyl-Zwischenprodukt.
- Entweder kann das trans-2-Decenoyl-Zwischenprodukt von FabB auf den normalen Syntheseweg für gesättigte Fettsäuren umgeleitet werden, wo die Doppelbindung hydrolysiert wird und das Endprodukt eine gesättigte Fettsäure ist, oder FabA katalysiert die Isomerisierung in die cis- 3-Decenoyl-Zwischenprodukt.
- FabB ist eine β-Ketoacyl-ACP-Synthase, die Zwischenprodukte verlängert und in den Mainstream-Fettsäuresyntheseweg kanalisiert. Wenn FabB mit dem cis-Decenoyl-Zwischenprodukt reagiert, ist das Endprodukt nach der Dehnung eine ungesättigte Fettsäure.
- Die beiden wichtigsten ungesättigten Fettsäuren sind Palmitoleoyl-ACP (16:1ω7) und cis-Vaccinoyl-ACP (18:1ω7).
Die meisten Bakterien, die einer anaeroben Entsättigung unterliegen, enthalten Homologe von FabA und FabB. Clostridien sind die Hauptausnahme; sie haben ein neues, noch zu identifizierendes Enzym, das die Bildung der cis-Doppelbindung katalysiert.
Verordnung
Dieser Weg unterliegt einer Transkriptionsregulation durch FadR und FabR. FadR ist das eingehender untersuchte Protein, dem bifunktionelle Eigenschaften zugeschrieben werden. Es wirkt als ein Aktivator von fabA und FABB Transkription und als Repressor für den β-Oxidations - Regulons . Im Gegensatz dazu fungiert FabR als Repressor für die Transkription von fabA und fabB.
Aerobe Entsättigung
Die aerobe Entsättigung ist der am weitesten verbreitete Weg zur Synthese ungesättigter Fettsäuren. Es wird in allen Eukaryoten und einigen Prokaryoten verwendet. Dieser Weg nutzt Desaturasen , um ungesättigte Fettsäuren aus gesättigten Fettsäuresubstraten voller Länge zu synthetisieren. Alle Desaturasen benötigen Sauerstoff und verbrauchen letztendlich NADH, obwohl die Entsättigung ein oxidativer Prozess ist. Desaturasen sind spezifisch für die Doppelbindung, die sie im Substrat induzieren. In Bacillus subtilis ist die Desaturase 5 -Des spezifisch für die Induktion einer cis-Doppelbindung an der 5 -Position. Saccharomyces cerevisiae enthält eine Desaturase, Ole1p, die die cis-Doppelbindung bei Δ 9 induziert .
Bei Säugern wird die aerobe Entsättigung durch einen Komplex aus drei membrangebundenen Enzymen katalysiert ( NADH-Cytochrom b 5 Reduktase, Cytochrom b 5 und eine Desaturase ). Diese Enzyme ermöglichen molekularem Sauerstoff, O 2 , mit der gesättigten Fettacyl-CoA-Kette zu interagieren, wodurch eine Doppelbindung und zwei Wassermoleküle, H 2 O, gebildet werden. Zwei Elektronen stammen von NADH + H + und zwei von der Einfachbindung im Fettsäurekette. Diese Säugetierenzyme sind jedoch nicht in der Lage, Doppelbindungen an Kohlenstoffatomen jenseits von C-9 in der Fettsäurekette einzuführen.. Daher können Säugetiere Linoleat oder Linolenat (die Doppelbindungen an C-12 (= Δ 12 ) haben ) nicht synthetisieren. oder an den Positionen C-12 und C-15 (= Δ 12 bzw. Δ 15 ) sowie an der 9- Position) noch die mehrfach ungesättigte Arachidonsäure mit 20 Kohlenstoffatomen , die von Linoleat abgeleitet ist. Diese werden alle als essentielle Fettsäuren bezeichnet , das heißt, sie werden vom Organismus benötigt, können aber nur über die Nahrung zugeführt werden. (Arachidonsäure ist die Vorstufe der Prostaglandine, die als lokale Hormone vielfältige Funktionen erfüllen .)
Ungeradkettige Fettsäuren
Ungerade Kettenfettsäuren (OCFAs) sind solche Fettsäuren , die eine ungerade Anzahl von Kohlenstoffatomen enthalten. Die gebräuchlichsten OCFAs sind die gesättigten C15- und C17-Derivate bzw. Pentadecansäure und Heptadecansäure . Die Synthese der geradkettigen Fettsäuresynthese erfolgt durch den Aufbau von Acetyl-CoA- Vorstufen, jedoch wird Propionyl-CoA anstelle von Acetyl-CoA als Primer für die Biosynthese von langkettigen Fettsäuren mit einer ungeraden Anzahl von Kohlenstoffatomen verwendet.
Regulation In B. subtilis wird dieser Stoffwechselweg durch ein Zweikomponentensystem reguliert : DesK und DesR. DesK ist eine membranassoziierte Kinase und DesR ist ein Transkriptionsregulator des des- Gens. Die Regelung reagiert auf Temperatur; bei einem Temperaturabfall wird dieses Gen hochreguliert. Ungesättigte Fettsäuren erhöhen die Fließfähigkeit der Membran und stabilisieren sie bei niedrigeren Temperaturen. DesK ist das Sensorprotein, das bei Temperaturabfall autophosphoryliert. DesK-P wird seine Phosphorylgruppe auf DesR übertragen. Zwei DesR-P-Proteine dimerisieren und binden an die DNA-Promotoren des des- Gens und rekrutieren RNA-Polymerase, um mit der Transkription zu beginnen.
Pseudomonas aeruginosa
Im Allgemeinen findet sowohl die anaerobe als auch die aerobe Synthese ungesättigter Fettsäuren nicht innerhalb desselben Systems statt, jedoch sind Pseudomonas aeruginosa und Vibrio ABE-1 Ausnahmen. Während P. aeruginosa hauptsächlich einer anaeroben Entsättigung unterliegt, durchläuft es auch zwei aerobe Wege. Ein Weg verwendet eine Δ 9 -Desaturase (DesA), die eine Doppelbindungsbildung in Membranlipiden katalysiert. Ein anderer Weg verwendet zwei Proteine, DesC und DesB, zusammen, um als Δ 9 -Desaturase zu wirken , die eine Doppelbindung in ein gesättigtes Fettsäure-CoA-Molekül einfügt. Dieser zweite Weg wird durch das Repressorprotein DesT reguliert. DesT ist auch ein Repressor der fabAB- Expression für die anaerobe Entsättigung in Gegenwart von exogenen ungesättigten Fettsäuren. Dies dient dazu, die Expression der beiden Wege innerhalb des Organismus zu koordinieren.
Verzweigtkettige Fettsäuren
Verzweigtkettige Fettsäuren sind normalerweise gesättigt und kommen in zwei verschiedenen Familien vor: der Iso-Reihe und der Anteiso-Reihe. Es wurde festgestellt, dass Actinomycetales einzigartige Mechanismen der Synthese von verzweigtkettigen Fettsäuren enthalten, einschließlich desjenigen, der Tuberculosterinsäure bildet.
System zur Synthese von verzweigtkettigen Fettsäuren
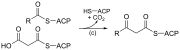
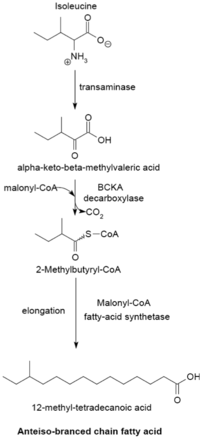
Das Synthesesystem für verzweigtkettige Fettsäuren verwendet α-Ketosäuren als Primer. Dieses System unterscheidet sich von der verzweigtkettigen Fettsäuresynthetase, die kurzkettige Acyl-CoA-Ester als Primer verwendet. α-Ketosäure-Primer werden aus der Transaminierung und Decarboxylierung von Valin , Leucin und Isoleucin abgeleitet , um 2-Methylpropanyl-CoA, 3-Methylbutyryl-CoA bzw. 2-Methylbutyryl-CoA zu bilden. Von Valin abgeleitete 2-Methylpropanyl-CoA-Primer werden verlängert, um geradzahlige Fettsäuren der Isoreihe wie 14-Methylpentadecansäure (Isopalmitinsäure) zu produzieren, und 3-Methylbutyryl-CoA-Primer aus Leucin können verwendet werden, um ungeradzahlige . zu bilden Fettsäuren der iso-Reihe, wie 13-Methyltetradecansäure. 2-Methylbutyryl-CoA-Primer von Isoleucin werden verlängert, um Fettsäuren der Anteiso-Reihe zu bilden, die eine ungerade Anzahl von Kohlenstoffatomen enthalten, wie 12-Methyltetradecansäure. Die Decarboxylierung der Primer-Vorläufer erfolgt durch das Enzym der verzweigtkettigen α-Ketosäuredecarboxylase (BCKA). Die Elongation der Fettsäure folgt dem gleichen Biosyntheseweg in Escherichia coli, der zur Herstellung von geradkettigen Fettsäuren verwendet wird, wobei Malonyl-CoA als Kettenverlängerer verwendet wird. Die wichtigsten Endprodukte sind verzweigtkettige Fettsäuren mit 12–17 Kohlenstoffatomen, deren Zusammensetzung für viele Bakterienarten einheitlich und charakteristisch ist.
BCKA-Decarboxylase und relative Aktivitäten von α-Ketosäure-Substraten
Das BCKA-Decarboxylase-Enzym besteht aus zwei Untereinheiten in einer tetrameren Struktur (A 2 B 2 ) und ist essentiell für die Synthese von verzweigtkettigen Fettsäuren. Es ist für die Decarboxylierung von α-Ketosäuren verantwortlich, die durch die Transaminierung von Valin, Leucin und Isoleucin gebildet werden, und produziert die Primer, die für die Synthese von verzweigtkettigen Fettsäuren verwendet werden. Die Aktivität dieses Enzyms ist bei verzweigtkettigen α-Ketosäure-Substraten viel höher als bei geradkettigen Substraten, und bei Bacillus- Arten ist seine Spezifität für die von Isoleucin abgeleitete α-Keto-β-methylvaleriansäure am höchsten, gefolgt von α- Ketoisocaproat und α-Ketoisovalerat. Die hohe Affinität des Enzyms zu verzweigtkettigen α-Ketosäuren ermöglicht es, als Primer-Donorsystem für die verzweigtkettige Fettsäuresynthetase zu fungieren.
| Substrat | BCKA-Aktivität |
CO 2 Produziert (nmol/min mg) |
Kilometer (μM) | Vmax (nmol/min mg) |
|---|---|---|---|---|
| L- α-Keto-β-methyl-valerat | 100% | 19,7 | <1 | 17,8 |
| α-Ketoisovalerat | 63 % | 12,4 | <1 | 13.3 |
| α-Ketoisocaproat | 38% | 7,4 | <1 | 5,6 |
| Pyruvat | 25% | 4.9 | 51,1 | 15,2 |
Faktoren, die Kettenlänge und Musterverteilung beeinflussen
α-Ketosäure-Primer werden verwendet, um verzweigtkettige Fettsäuren herzustellen, die im Allgemeinen zwischen 12 und 17 Kohlenstoffatomen lang sind. Die Anteile dieser verzweigtkettigen Fettsäuren neigen dazu, unter einer bestimmten Bakterienart einheitlich und konsistent zu sein, können jedoch aufgrund von Änderungen der Malonyl-CoA-Konzentration, der Temperatur oder der vorhandenen hitzestabilen Faktoren (HSF) verändert werden. Alle diese Faktoren können die Kettenlänge beeinflussen, und es wurde gezeigt, dass HSFs die Spezifität der BCKA-Decarboxylase für ein bestimmtes α-Ketosäure-Substrat verändern, wodurch das Verhältnis der produzierten verzweigtkettigen Fettsäuren verschoben wird. Es hat sich gezeigt, dass eine Erhöhung der Malonyl-CoA-Konzentration zu einem größeren Anteil an C17-Fettsäuren führt, bis die optimale Konzentration (≈20 μM) von Malonyl-CoA erreicht ist. Erniedrigte Temperaturen neigen auch dazu, die Fettsäureverteilung bei Bacillus- Spezies leicht in Richtung C17-Fettsäuren zu verschieben.
Verzweigtkettige Fettsäuresynthase
Dieses System funktioniert ähnlich wie das System zur Synthese von verzweigtkettigen Fettsäuren, verwendet jedoch anstelle von Alpha-Ketosäuren kurzkettige Carbonsäuren als Primer. Im Allgemeinen wird diese Methode von Bakterien verwendet, die nicht die Fähigkeit haben, das verzweigtkettige Fettsäuresystem unter Verwendung von Alpha-Keto-Primern durchzuführen. Typische kurzkettige Primer umfassen Isovalerat, Isobutyrat und 2-Methylbutyrat. Die für diese Grundierungen benötigten Säuren werden in der Regel aus der Umwelt aufgenommen; dies wird häufig bei Pansenbakterien beobachtet.
Die Gesamtreaktion ist:
- Isobutyryl-CoA + 6 Malonyl-CoA +12 NADPH + 12H + → Isopalmitinsäure + 6 CO 2 12 NADP + 5 H 2 O + 7 CoA
Der Unterschied zwischen (geradkettiger) Fettsäuresynthase und verzweigtkettiger Fettsäuresynthase ist die Substratspezifität des Enzyms, das die Reaktion von Acyl-CoA zu Acyl-ACP katalysiert.
Omega-alizyklische Fettsäuren
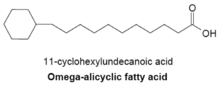
Omega-alicyclische Fettsäuren enthalten typischerweise eine omega-terminale cyclische Propyl- oder Butyrylgruppe und sind einige der wichtigsten Membranfettsäuren, die in mehreren Bakterienarten vorkommen. Die Fettsäuresynthetase, die zur Herstellung von Omega-alizyklischen Fettsäuren verwendet wird, wird auch verwendet, um membranverzweigte Fettsäuren herzustellen. Bei Bakterien mit Membranen, die hauptsächlich aus omega-alicyclischen Fettsäuren bestehen, ist das Angebot an cyclischen Carbonsäure-CoA-Estern viel größer als bei verzweigtkettigen Primern. Die Synthese von zyklischen Primern ist nicht gut verstanden, aber es wurde vorgeschlagen, dass der Mechanismus die Umwandlung von Zuckern in Shikimisäure beinhaltet, die dann in Cyclohexylcarbonsäure-CoA-Ester umgewandelt wird, die als Primer für die Synthese von Omega-alizyklischen Fettsäuren dienen
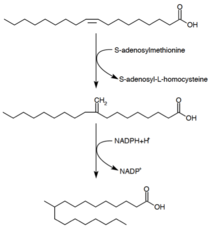
Synthese von Tuberkulostearinsäure
Tuberkulostearinsäure ( D -10-Methylstearinsäure) ist eine gesättigte Fettsäure, von der bekannt ist, dass sie von Mycobacterium spp. produziert wird . und zwei Arten von Streptomyces . Es wird aus der Vorstufe Ölsäure (einer einfach ungesättigten Fettsäure) gebildet. Nachdem Ölsäure zu einem Phospholipid verestert ist, spendet S-Adenosyl-Methionin eine Methylgruppe an die Doppelbindung der Ölsäure. Diese Methylierungsreaktion bildet das Zwischenprodukt 10-Methylen-Octadecanoyal. Sukzessive Reduktion des Rückstands mit NADPH als Cofaktor führt zu 10-Methylstearinsäure