Glycerinaldehyd - Glyceraldehyde

|
|

|
|
| Namen | |
|---|---|
|
IUPAC-Name
Glycerinaldehyd
|
|
|
Systematischer IUPAC-Name
2,3-Dihydroxypropanal |
|
| Andere Namen
Glycerinaldehyd
Glycerinaldehyd Glycerin |
|
| Kennungen | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.000,264 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| C 3 H 6 O 3 | |
| Molmasse | 90,078 g · mol –1 |
| Dichte | 1,455 g / cm 3 |
| Schmelzpunkt | 145 ° C (293 ° F; 418 K) |
| Siedepunkt | 140 bis 150 ° C (284 bis 302 ° F; 413 bis 423 K) bei 0,8 mmHg |
|
Sofern nicht anders angegeben, werden Daten für Materialien in ihrem Standardzustand (bei 25 ° C, 100 kPa) angegeben. |
|
|
|
|
| Infobox-Referenzen | |
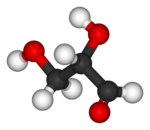
Glycerinaldehyd ( Glycerin ) ist ein Triose- Monosaccharid mit der chemischen Formel C 3 H 6 O 3 . Es ist die einfachste aller gängigen Aldosen . Es ist ein süßer , farblose, kristalliner Feststoff , der eine Zwischenverbindung in ist Kohlenhydratstoffwechsel . Das Wort stammt aus der Kombination von Glycerin und Aldehyd , da Glycerinaldehyd Glycerin mit einer zu einem Aldehyd oxidierten Alkoholgruppe ist .
Struktur
Glycerinaldehyd hat ein chirales Zentrum und liegt daher als zwei verschiedene Enantiomere mit entgegengesetzter optischer Rotation vor:
- In der D / L- Nomenklatur bedeutet entweder D aus dem lateinischen Dexter "rechts" oder L aus dem lateinischen Laevo "links".
- In der R / S-Nomenklatur bedeutet entweder R vom lateinischen Rectus "rechts" oder S vom lateinischen Sinister "links".
|
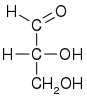
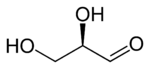
D -glyceraldehyde ( R ) -glyceraldehyde (+) - Glycerinaldehyd |
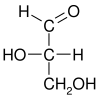
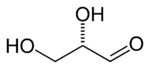
L -glyceraldehyde ( S ) -glyceraldehyde (-) - Glycerinaldehyd |
|
| Fischer-Projektion |
|
|
| Skelettformel |
|
|
| Ball-and-Stick-Modell |

|
|
Während die optische Drehung von Glycerinaldehyd für R (+) und für S (-) ist , gilt dies nicht für alle Monosaccharide. Die stereochemische Konfiguration kann nur aus der chemischen Struktur bestimmt werden, während die optische Drehung nur empirisch (experimentell) bestimmt werden kann.
Glücklicherweise wurde die molekulare D- Geometrie im späten 19. Jahrhundert (+) - Glycerinaldehyd zugeordnet, wie durch Röntgenkristallographie im Jahr 1951 bestätigt wurde.
Nomenklatur
Im D / L- System wird Glycerinaldehyd als Konfigurationsstandard für Kohlenhydrate verwendet. Monosaccharide mit einer absoluten Konfiguration, die mit ( R ) -Glycerinaldehyd im letzten Stereozentrum identisch ist , beispielsweise C5 in Glucose , werden dem Stereodeskriptor D- zugeordnet . Den ( S ) -Glycerinaldehyd ähnlichen wird ein L- zugeordnet .
Chemische Synthese
Glycerinaldehyd hergestellt werden kann, zusammen mit Dihydroxyaceton , durch die milde Oxidation von Glycerin , beispielsweise mit Wasserstoffperoxid und ein Eisensalz als Katalysator . Dihydroxyaceton, die einfachste Ketose , ist ein Isomer von Glycerinaldehyd.
Biosynthese
Das Enzym Glycerindehydrogenase (NADP + ) hat zwei Substrate, Glycerin und NADP + , und drei Produkte, D-Glycerinaldehyd, NADPH und H + .
Biochemische Rolle
Die durch das Enzym Triosephosphatisomerase katalysierte Umwandlung der Phosphate von Glycerinaldehyd ( Glycerinaldehyd-3-phosphat ) und Dihydroxyaceton ( Dihydroxyacetonphosphat ) ist ein wichtiger Zwischenschritt bei der Glykolyse .
