Alamethicin - Alamethicin

|
|
| Namen | |
|---|---|
|
IUPAC-Name
N- Acetyl-2- methylalanyl- L- Prolyl-2-Methylalanyl- L- Alanyl-2-Methylalanyl- L- Alanyl- L - Glutaminyl -2-Methylalanyl- L- Valyl-2-Methylalanylglycyl- L- Leucyl-2- Methylalanyl- L -prolyl- L -valyl-2-methylalanyl-2-methylalanyl- L -α-glutamyl- N 1 -[(1 S )-1-Benzyl-2-hydroxyethyl]- L -glutamamid
|
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA-Infokarte |
100.121.626 |
|
PubChem- CID
|
|
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| C 92 H 150 N 22 O 25 | |
| Molmasse | 1964,31 g/mol |
| Aussehen | Weißer Feststoff |
| Schmelzpunkt | 255 bis 270 °C (491 bis 518 °F; 528 bis 543 K) |
| Unlöslich | |
| Löslichkeit in DMSO , Methanol , Ethanol | Löslich |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
Alamethicin ist ein kanalbildendes Peptid antibiotische , produziert von dem Pilz Trichoderma viride . Es gehört zu den Peptaibol- Peptiden, die den nicht-proteinogenen Aminosäurerest Aib ( 2-Aminoisobuttersäure ) enthalten. Dieser Rest induziert stark die Bildung einer alpha-helikalen Struktur. Die Peptidsequenz ist:
Ac-Aib-Pro-Aib-Ala-Aib-Ala-Gln-Aib-Val-Aib-Gly-Leu-Aib-Pro-Val-Aib-Aib-Glu-Gln-Phl
(Ac = Acetyl, Phl = Phenylalaninol , Aib = 2-Aminoisobuttersäure )
In Zellmembranen , bildet es Spannung -abhängigen Ionenkanäle durch Aggregation von vier bis sechs Molekülen .
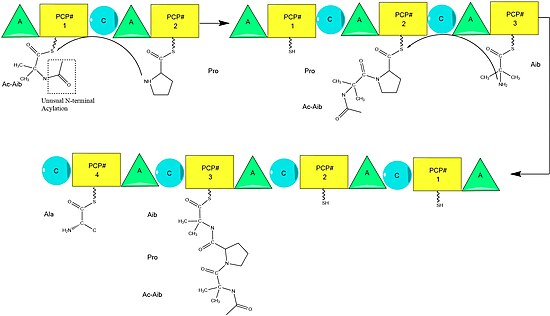
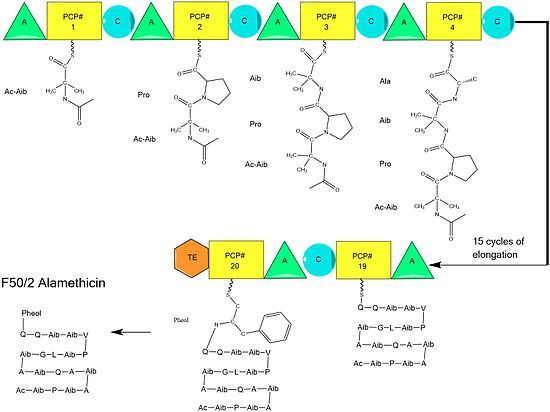
Biosynthese
Es wird angenommen, dass die Alamethicin-Biosynthese durch die Alamethicin-Synthase katalysiert wird, eine 1975 erstmals isolierte nichtribosomale Peptid- Synthase (NRPS). Obwohl mehrere Sequenzen des Alamethicin-Peptids akzeptiert werden, deuten Hinweise darauf hin, dass diese alle dem allgemeinen NRPS-Mechanismus mit kleinen Variationen an ausgewählten Aminosäuren folgen . Beginnend mit der Acylierung des N-Terminus der ersten Aminoisobuttersäure am ALM-Synthase-Enzym durch Acetyl-CoA folgt die sequentielle Kondensation von Aminosäuren durch jede modulare Einheit der Synthetase. Aminosäuren werden zunächst durch einen „adenyliert Adenylylierung “ (A) Bereich durch eine vor angebracht ist Thioester - Bindung an einem Acylträgerprotein -ähnlichen Peptidyl Trägerprotein. Die wachsende Kette wird durch die "Kondensation" (C)-Domäne an das Aminosäure-tragende PCP angehängt, gefolgt von einer weiteren Runde der gleichen Reaktionen durch das nächste Modul.
Der Zusammenbau wird durch Zugabe von Phenylalaninol, einem ungewöhnlichen Aminosäure-ähnlichen Substrat, abgeschlossen. Nach Zugabe von Phenylalaninol wird die fertige Peptidkette durch die Thioesterasedomäne gespalten, wobei die Thioesterbindung gespalten wird und ein Alkohol zurückbleibt.
Verweise
Weiterlesen
- Jones, LR; Maddock, SW; Besch, HR Jr. (1980). „Demaskierende Wirkung von Alamethicin auf die (Na+,K+)-ATPase, beta-adrenerge Rezeptor-gekoppelte Adenylatzyklase und cAMP-abhängige Proteinkinase-Aktivitäten von kardialen Sarkolemmalvesikeln“ . J. Biol. Chem . 255 (20): 9971–9980. doi : 10.1016/S0021-9258(18)43488-6 . PMID 6253461 .
- Erkunden Sie die Strukturen von Alamethicin in der Proteindatenbank
-
Alamethicin in Norine
- Aus "Ein spannungsgesteuertes Ionenkanalmodell, das aus der Kristallstruktur von Alamethicin bei einer Auflösung von 1,5 A abgeleitet wird." Fox Jr., RO; Richards, FM (1982). „Ein spannungsgesteuertes Ionenkanalmodell, das aus der Kristallstruktur von Alamethicin bei 1,5-A-Auflösung abgeleitet wird“. Natur . 300 (5890): 325–30. Bibcode : 1982Natur.300..325F . doi : 10.1038/300325a0 . PMID 6292726 . S2CID 4278453 .
- Leitgeb, Balázs; Szekeres, András; Manczinger, László; Vágvölgyi, Csaba; Kredics, László (2007-06-01). „Die Geschichte von Alamethicin: Eine Überprüfung der am umfangreichsten untersuchten Peptaibol“. Chemie & Biodiversität . 4 (6): 1027–1051. doi : 10.1002/cbdv.200790095 . ISSN 1612-1880 . PMID 17589875 . S2CID 40886688 .